
记者3月17日从中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)获悉,该中心联合海军军医大学第二附属医院,在国际上首次分别利用自体与异体干细胞来源的再生胰岛微创移植,实现了1型糖尿病患者的胰岛功能重建与血糖自主调控。相关论文发表于国际学术期刊《柳叶刀·糖尿病与内分泌学》。
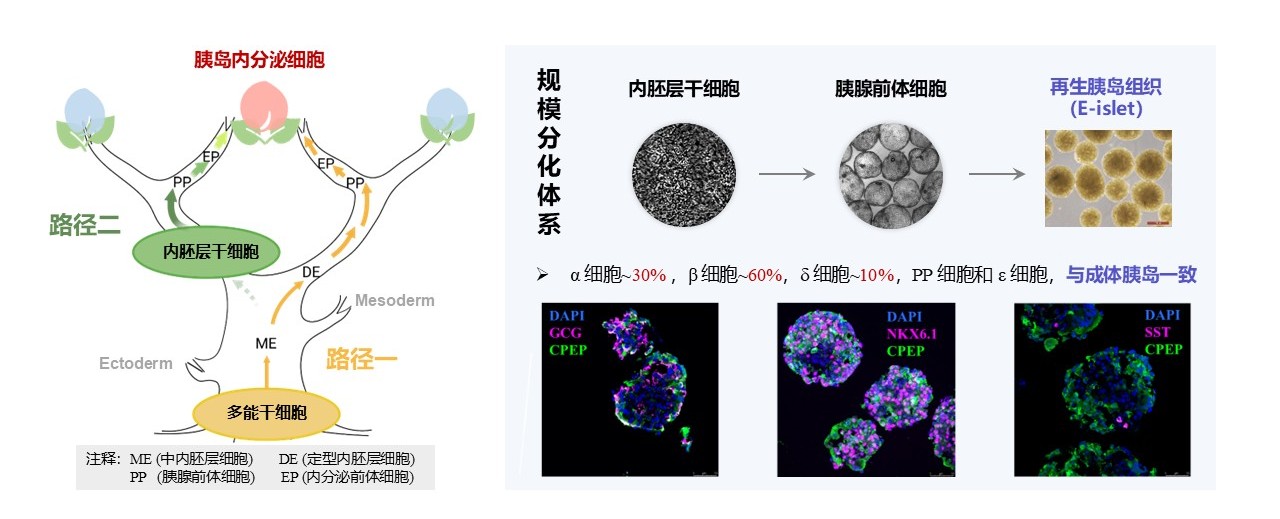
基于内胚层干细胞的胰岛体外再造技术。
“零件”再造,开辟全新技术路径
糖尿病是严重威胁我国居民健康的慢性病,其中1型糖尿病多发病于儿童及青少年。由于自身免疫紊乱、机体免疫系统异常攻击并破坏胰岛β细胞,导致胰岛功能衰竭、胰岛素分泌严重不足、血糖难以控制,1型糖尿病长期以来被视作无法逆转的慢性疾病。患者必须终身依赖胰岛素注射与频繁血糖监测,还可能引发严重并发症。传统的胰岛移植虽有效,但受限于供体严重匮乏,无法惠及广大患者。如何实现胰岛组织的规模化再生,成为全球医学界亟待攻克的难题。
体外胰岛再生,相当于给患者“更换零件”。常规方法使用的原材料,是“多能干细胞”。它就像一棵树的“树根”,理论上可以发育成人体各种各样的细胞类型,潜力巨大。但从树根到开花结果,长成人体需要的胰岛组织,中间要经历非常复杂的分枝散叶的过程,步骤多,路线长,而且在体外很难精准调控,生产出来的产品纯度不够高,还可能混入具有体内增殖能力、未完全分化的细胞,带来成瘤风险。
据中国科学院分子细胞科学卓越创新中心研究员程新介绍,研究团队经过二十多年的深入研究,另辟蹊径,建立了一套全新的“基于内胚层干细胞的技术体系”,不再从“树根”出发,而是直接从“树干”上的特定位置——“内胚层干细胞”开始定向分化。
这一新“起点”优势明显:分化方向更明确,从初始阶段就设置了导航路线,只朝胰腺、肝脏这类内胚层来源的细胞前进,不会偏航成其他类型的细胞;其次,分化步骤从十步精简到两步,生产周期从5~6周缩短为2周,流程简化的同时大大提升了效率。最重要的是,内胚层干细胞在体内不会增殖,最大程度地降低了传统方法可能带来的体内成瘤风险。
利用这项全球领先的体外定向分化技术,团队成功构建了可用于治疗胰岛功能严重受损/衰竭型糖尿病的“再生胰岛”(E-islet)。再生胰岛经肝门静脉输注到患者体内后,它们就能像正常胰岛组织一样,发挥调控血糖的功能。
临床攻坚,三例患者见证胰岛功能重建
研究团队在三例1型糖尿病患者中,分别采用自体或异体内胚层干细胞来源的再生胰岛开展临床研究,并在不同免疫抑制策略下评估疗效与安全性,临床数据令人振奋。3个临床病例涵盖了世界首例自体与中国首例异体再生胰岛移植治疗1型糖尿病,以及世界首例再生胰岛移植治疗青少年1型糖尿病的情况,其中最长一例已实现临床治愈超过26个月。
研究团队首次在国际上证明了,无论是自体还是异体来源的再生胰岛移植,均可在1型糖尿病患者中实现胰岛功能重建、血糖自主调控与外源胰岛素脱离,从而长期改善患者的血糖水平、有效避免并发症的发生与进展。研究提示,该疗法目前仍需联合使用长期免疫抑制治疗,用于克服1型糖尿病自身免疫复发等问题。
基于该自主知识产权开发的“异体人再生胰岛注射液(E-islet 01)”已于2025年4月和2026年1月先后获得中国和美国的新药临床试验(IND)批件。目前,临床试验正在严谨有序地开展,进展顺利。
为避免长期使用免疫抑制剂带来的潜在随机感染和恶变风险,研究团队未来将进一步筛选更精准的免疫抑制方案,同时开发具备免疫逃逸功能的、不再需要免疫制剂的、安全可控的“广义通用型”再生胰岛产品,以期惠及广大的糖尿病患者。
新京报记者 张璐
编辑 张牵 校对 柳宝庆





