全文共计999字 | 看完大概需要5分钟
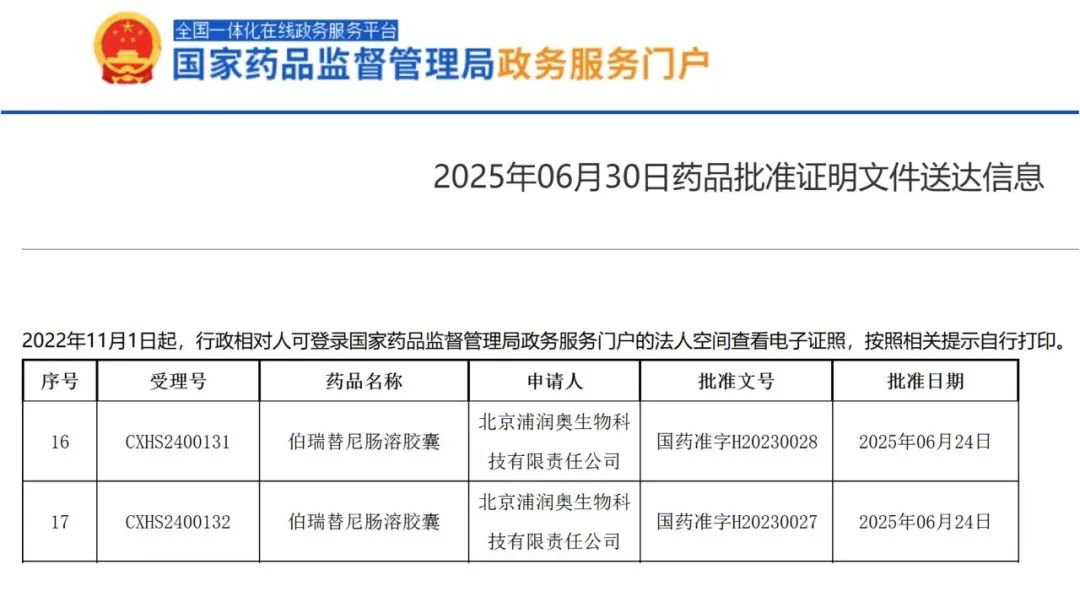
大兴区融媒体中心消息 6月30日,大兴区生物医药企业北京鞍石生物科技股份有限公司(以下简称“鞍石生物科技”)全资子公司——北京浦润奥生物科技有限责任公司自主研发的MET抑制剂伯瑞替尼肠溶胶囊(商品名:万比锐,以下简称“伯瑞替尼”)获中国国家药品监督管理局(NMPA)附条件批准,用于治疗具有间质-上皮转化因子(MET)扩增的局部晚期或转移性非小细胞肺癌(NSCLC)患者。
据介绍,这是伯瑞替尼在中国获批的第三个适应症,也是全球首个获批的单药治疗MET扩增NSCLC患者的适应症,预示着MET扩增NSCLC进入精准靶向治疗时代。2024年12月25日,鞍石生物科技向中国国家药品监督管理局药品审评中心递交了该适应症NDA申请,获正式受理并被纳入优先审评。
记者了解到,在非小细胞肺癌(NSCLC)中,MET异常存在多种类型,发生率及临床意义均有差异,需要精准识别。MET基因扩增作为NSCLC驱动基因之一,其发生率为1%~5%,为明确的靶向治疗标志物。浙江大学医学院附属第一医院教授周建娅表示,目前国内对于MET扩增尚无治疗推荐,多参考无驱动基因治疗方案,疗效不佳,临床急需新型靶向治疗方案。
广东省人民医院教授吴一龙介绍,伯瑞替尼此次在我国获批用于治疗具有间质-上皮转化因子(MET)扩增的局部晚期或转移性非小细胞肺癌患者适应症,是基于KUNPENG(NCT04258033)研究中队列2及队列3的积极研究结果。KUNPENG研究是伯瑞替尼治疗 MET异常的晚期 NSCLC患者有效性和安全性的一项多中心、多队列、开放标签注册临床Ⅱ期研究。队列2主要纳入标准治疗(含铂化疗方案)失败的MET扩增经治患者;队列3主要纳入患者拒绝化疗的MET扩增初治患者。
研究表明,伯瑞替尼治疗86例MET扩增NSCLC患者,总人群客观缓解率(ORR)达48.8%,中位无进展生存期(PFS)7.4个月,中位总生存期(OS)13.9个月,显示出显著疗效。值得注意的是,在21例基线脑转移患者中,伯瑞替尼展现出良好的颅内活性,其对脑转移患者具有明确的临床治疗价值。
此前,伯瑞替尼肠溶胶囊于2023年11月在中国获得附条件批准,用于治疗具有间质-上皮转化因子(MET)外显子14跳变的局部晚期或转移性非小细胞肺癌患者。2024年4月获批用于既往治疗失败的具有PTPRZ1-MET融合基因的IDH突变型星形细胞瘤(WHO 4级)或有低级别病史的胶质母细胞瘤成人患者。
记者:张冕群
编辑:周露
审核:厉春 王剑秋
签发:杨理光



特别声明:本文为新京报客户端新媒体平台"新京号"作者或机构上传并发布,仅代表该作者或机构观点,不代表新京报的立场及观点。新京报仅提供信息发布平台。